 更多“强碱滴定弱酸,当酸的浓度一定时,Ka与突跃范围的关系是什么?”相关的问题
更多“强碱滴定弱酸,当酸的浓度一定时,Ka与突跃范围的关系是什么?”相关的问题
第2题
准确量取30.00ml弱酸,加水稀释至100ml。以为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被
准确量取30.00ml弱酸,加水稀释至100ml。以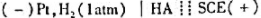 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。
第5题
下列判断正确的是()
A.做焰色反应时,火焰呈紫色,一定是钾盐
B.17g羟基中含有质子数10NA
C.78g过氧化钠与足量的水反应,电子转移数1NA
D.标准酸滴定未知浓度碱时,水的电离程度最大时应是PH=7时
E.短周期某元素的氧化物既能与强酸反应又能与强碱反应,该元素可能是铝或硅
第6题
下列物质(均为0.1mol/L),不能用强碱标准溶液直接滴定的是()。
A.一氯醋酸(Ka=1.4x10-3)
B.邻苯二甲酸氢钾(Ka1=3.1x10-6)
C.苯酚(Ka=1.3x10-10)
D.NH4Cl(KNH3=1.8x10-5)
第7题
用同一NaOH标准溶液滴定相同浓度的不同一元弱酸时,若弱酸的解离常数越大,则()。A、消耗NaOH标准
用同一NaOH标准溶液滴定相同浓度的不同一元弱酸时,若弱酸的解离常数越大,则()。A、消耗NaOH标准
点击查看答案
用同一NaOH标准溶液滴定相同浓度的不同一元弱酸时,若弱酸的解离常数 越大,则()。
越大,则()。
A、消耗NaOH标准溶液的体积越大
B、消耗NaOH标准溶液的体积越小
C、滴定突跃范围越大
D、滴定突跃范围越小
第11题
298K时,用0.1000mol/LNaOH溶液滴定20.00mL同浓度的甲酸溶液过程中溶液PH与NaOH溶液体积的关系如图所示(已知:HCOOH溶液的Ka=l.0×10-4.0),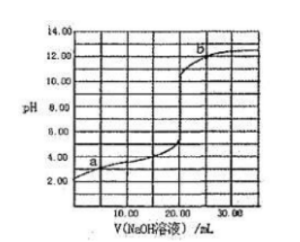 下列有关叙述正确的是()。
下列有关叙述正确的是()。
A.该滴定过程应该选择甲基橙作为指示剂
B.图中a,b两点水的电离程度:b>a
C.当加入10.00mLNaOH溶液时,c(HCOO-)>c(H+)>c(Na+)>c (OH-)
D.当加入20.00mLNaOH溶液时,溶液pH>8.0


 如果结果不匹配,请
如果结果不匹配,请 
















