 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[Co(NH3)6]3+是内轨型配合物,则其中心离子未成对电子数和杂化轨道类型是()。A.4,sp3d2B.0,sp3
[Co(NH3)6]3+是内轨型配合物,则其中心离子未成对电子数和杂化轨道类型是()。
A.4,sp3d2
B.0,sp3d2
C.4,d2sp3
D.0,d2sp3
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[Co(NH3)6]3+是内轨型配合物,则其中心离子未成对电子数和杂化轨道类型是()。
A.4,sp3d2
B.0,sp3d2
C.4,d2sp3
D.0,d2sp3
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“[Co(NH3)6]3+是内轨型配合物,则其中心离子未成对电…”相关的问题
更多“[Co(NH3)6]3+是内轨型配合物,则其中心离子未成对电…”相关的问题
已知下列配合物的分裂能(△。)和中心离子的电子成对能(P),写出各中心离子的d电子排布式,并估算它们的磁矩各为多少。指出这些配合物中何者为高自旋型,何者为低自旋型?
配离子 (1)[Co(NH3)6]2+(2) [Fe(H2O)6]2+(3)[Co(NH3)6]3+
P/cm-122500 17600 21000
△。/cm-111000 1040O 22900
根据实验测得的有效磁矩,试确定下列配合物是内轨型还是外轨型,说明理由,并以它们的电子层结构表示。
(1)[Mn(SCN)6]4-,μ=6.1 B.M.;
(2)[Mn(CN)6]4-,μ=1.8 B.M.;
(3)[Co(NO2)6]3-,μ=0 B.M.;
(4)[Co(SCN)4]2-,μ=4.3 B.M.;
(5)K3[FeF6],μ=5.9 B.M.;
(6)K3[Fe(CN)6],μ=2.3 B.M.。
A.Ni(CO)4和[Ni(CN)4]2-中,镍元素均是sp3杂化
B.NH3的空间构型为平面三角形
C.O与CN-互为等电子体,其中CO分子内σ键和π键个数之比为1:2
D.Ni2+在形成配合物时,其配位数只能为4
配合物[Co(NH3)4(H2O)2](SO4)3的内界是(),外界是(),配位体是()、配位原子是(),中心原子的配位数是()。
(1)根据电极点位表数据计算反应:
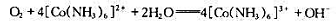
的平衡常数K.
(2)现将空气(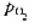 =20.3kPa)通入到含有0.10mol·dm-3[Co(NH3)6]3+,0.10mol·dm-3
=20.3kPa)通入到含有0.10mol·dm-3[Co(NH3)6]3+,0.10mol·dm-3
[Co(NH3)6]3+,2.0mol·dm-3NH2+及2.0mol·dm-3NH3·H2O的混合溶液中,能否发生上述反应?
配合物[Co(NH3)4(H2O)Cl]Cl2命名为______,该配合物磁矩为4.9μB,按价键理论,中心原子杂化类型为______,空间构型为______;按晶体场理论,中心原子电子排布为______,晶体场稳定化能为______Dq(或△0)。