 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298.15K时反应2Cu(s)+½O2(g)=Cu2O(s)中Cu、O2、Cu2O的分别为33.2、205.2、93.1,则该反应的为()。
A.-75.9
B.75.9
C.-145.3
D.145.3
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.-75.9
B.75.9
C.-145.3
D.145.3
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知298.15K时反应2Cu(s)+½O2(g)=Cu2O…”相关的问题
更多“已知298.15K时反应2Cu(s)+½O2(g)=Cu2O…”相关的问题
已知298.15K时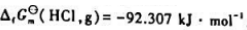 化学反应
化学反应
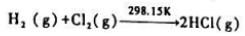
在催化剂的作用下反应速率大大加快时,反应的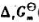 (298.15K)=().
(298.15K)=().
已知298.15K时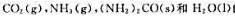 的标准摩尔生成焓和标准摩尔熵如下表所示:
的标准摩尔生成焓和标准摩尔熵如下表所示:

试通过计算判断下列反应
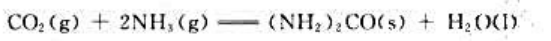
在298.15K、标准状态下能否自发进行。上述反应在标准状态下自发进行的最高温度是多少?
A.193kJ·mol-1
B.873kJ·mol-1
C.-193kJ·mol-1
D.-873kJ·mol-1
298.15K时,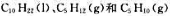 的标准摩尔燃烧焓分别为-6752kJ·mol- 1、-3492kJ·mol-1和-3364kJ·mol-1。计算298.15K裂解反应
的标准摩尔燃烧焓分别为-6752kJ·mol- 1、-3492kJ·mol-1和-3364kJ·mol-1。计算298.15K裂解反应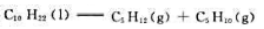 的标准摩尔焓变。
的标准摩尔焓变。
s)=H3(g)+H2S(g).容器内的总压是66.7kPa,一些固体,NH4HS保留在容器中.计算:(1)298.15K时的K值;(2)固体,NH4HS的分解率;(3)如果容器体积减半,容器中周体,NH4HS物质的量如何变化?
电池Ag(s)AgCl(s)]KCl(m)|Hg2Cl2(s)|HIg(I)的电池反应为
Ag(s)+1/2Hg2CI2(s)→AgCl(s)+Hg(I),已知298K时,此电池反应的焓变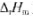 为5435/mol,各物质的规定熵数据为
为5435/mol,各物质的规定熵数据为
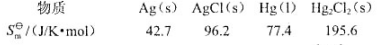 试计算该温度下电池的电动势E及电池电动势的温度系数
试计算该温度下电池的电动势E及电池电动势的温度系数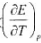
在298.15K及pΘ下,C(金刚石)和C(石墨)的SΘm值分别为2.38
5.74J.mol-1K-1,其ΔcHΘm值依次为-395.4kJ·mol-1和-393.51kJ·mol-1,求:
(1)在298.15K及pΘ下,石墨→金刚石的 值.
值.
(2)通过计算说明哪一种晶形较为稳定.
298.15K时,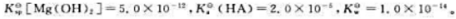 则下列化学反应
则下列化学反应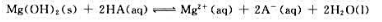 在298.15K时的标准平衡常数为()。
在298.15K时的标准平衡常数为()。
A、1.0×102
B、2.0×107
C、5.0×10-8
D、2.0×107