 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在25.00ml含Ni2+、Zn2+的溶液中加入5000ml,0.01500mol/LEDTA溶液,用0.01000mol/LM
g2+返滴定过量的EDTA,用去17.52ml,然后加入二巯基丙醇解蔽Zn2+,释放出EDTA,再用去2200mlMg2+溶液滴定。计算原试液中Ni2+、Zn2+的浓度。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在25.00ml含Ni2+、Zn2+的溶液中加入5000ml…”相关的问题
更多“在25.00ml含Ni2+、Zn2+的溶液中加入5000ml…”相关的问题
含H2SO4(Mr=98.07)和H3PO4(Mr=98.00)的混合液两份(体积均为25.00mL),分别用0.1018mol·L-1的NaOH标准溶液滴定。第一份以甲基橙(pKHn=3.4)作指示剂,需25.18mL 滴至终点;第二份以酚酞(pKHn=9.1)作指示剂,需35.22mL到达终点。试求混合液中每种酸的浓度?(已知H3PO4的Ka1=10-2.12,Ka2=10-7.21,Ka3=10-12.7)
mol·L-1EDTA.试计算SO42-的质量分数.

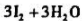 ,析出的碘用Na2S2O3溶液滴定,用去25.10ml。求:Na2S2O3溶液的浓度。(MHNO3=214.0)
,析出的碘用Na2S2O3溶液滴定,用去25.10ml。求:Na2S2O3溶液的浓度。(MHNO3=214.0)
肉类经烹调能释放出肌溶蛋白、肌肽、肌酸、肌酐、嘌呤碱和氨基酸等物质,总称为含N渗浸出物。()
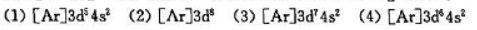
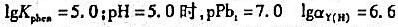 )
)
Co2+与SCN-生成蓝色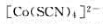 若溶液也含Fe3+,为避免[Fe(NCS)n]3-n的红色干扰,可在溶液中加入NaF、将Fe3+掩蔽起来。这是由于生成了()。
若溶液也含Fe3+,为避免[Fe(NCS)n]3-n的红色干扰,可在溶液中加入NaF、将Fe3+掩蔽起来。这是由于生成了()。
A.难溶的FeF3
B.难解离的FeF3
C.难解离的[FeFi6]-
D.难溶的Fe(SCN)F2