 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知条件如下:砂浆含水率为16.5%,滤纸吸水前后质量差为8.5g,砂浆样本质量为406g,试计算砂浆保水性()。
A.87.3%
B.88.4%
C.97.5%
D.97.9%
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.87.3%
B.88.4%
C.97.5%
D.97.9%
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知条件如下:砂浆含水率为16.5%,滤纸吸水前后质量差为8…”相关的问题
更多“已知条件如下:砂浆含水率为16.5%,滤纸吸水前后质量差为8…”相关的问题
在pH值为10.0的氨性溶液中,含Zn2+和Mg2+各0.020mol·L-1,用0.020mol·L-1EDTA溶液滴定Zn2+时,Mg2+是否干扰测定:______(填是与否)。若有干扰,应如何改变滴定条件:______。(设△pZn'=0.2,并要求滴定误差|Et|≤0.3%;已知化学计量点时[NH3]=0.20 mol·L-1,lgKZnY=16.5,lgKMgY=8.7。)
工厂购买了一台板框压滤机,规格为500×500×25mm。过滤条件:每次恒压过滤2h得滤液2m3,滤渣厚25mm,已知实验室事前在上述相同条件下进行实验,测得过滤常数K=1.43×10-3m2·min-1,qe=1.5×10-3m3·m-2,问:
某废催化剂主要成分有SiO2、ZnO、ZnS和CuS。某化学兴趣小组拟用该废催化剂为原料,制备硫酸锌和硫酸铜晶体。采用的实验方案如下,下列说法正确的是()。 已知:ZnS与稀硫酸发生反应且化合价不变,CuS既不溶于稀硫酸也不和稀硫酸反应
A.第一次浸出可以在烧杯中进行
B.第二次浸出时发生反应为CuS+H2O2+H2SO4=CuSO4+S+2H2O
C.滤渣2中只有二氧化硅
D.获得硫酸锌和硫酸铜晶体采用蒸发结晶的方式
工业上以锂辉石(Li2O·A12O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下: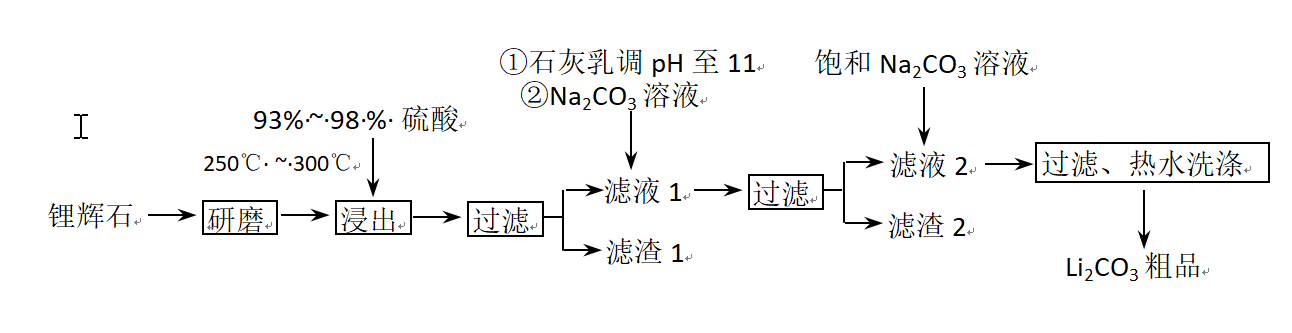 已知:①
已知:①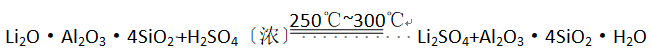 ②某些物质的溶解度(S)如下表所示
②某些物质的溶解度(S)如下表所示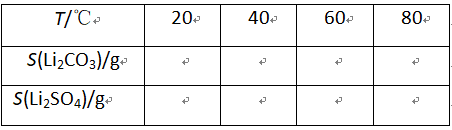
问题一、从滤渣1中别离出Al2O3的部分流程如以下图所示,括号表示加入的试剂,方框表示所得到的物质。则步骤Ⅱ中反应的离子方程式是()。
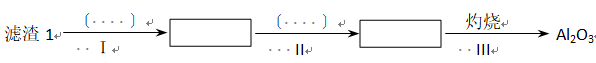
问题二、已知滤渣2的主要成分有Mg(OH)2和CaCO3向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)()
问题三、向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是()
问题四、工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下()
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3
①a中,阳极的电极反应式是()。
②b中,生成Li2CO3反应的化学方程式是()。
用BMS50/810-25(38个框)板框压滤机过滤含CaCO3的水悬浮液。已知条件为:料浆中固相质量分率为13.9%,滤饼中水的质量分率为32%,且每m3滤饼含固相1180kg。在200KPa下测得恒压过滤方程式为(q+3.45×10-3)2=2.72×10-5(θ+0.439)式中θ的单位为s。试计算。 (1)滤饼充满滤框所需时间;(2)滤毕,用1m3清水于过滤终了相同条件下洗涤,所需洗涤时间;(3)每批操作的辅助时间30min,生产能力Q(m3滤液/h)。
A.5%~10%
B.10%~15%
C.15%~20%
D.20%~25%
A.0万元
B.1.5万元
C.15万元
D.16.5万元
在pH=10.0的氨性缓冲溶液中,以0.020mol/L EDTA滴定相同浓度的Zn2+,已知lgKZnY=16.5,lgαY(H)=0.5,lgαZn(NH3)=5.0,lgαZn(OH)=2.4,则化学计量点时pZn'值为( )
A.6.5
B.8.0
C.11.5
D.10.0
A.2.1%
B.14.0%
C.86.0%
D.97.90%