 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应(1)和反应(2)具有相同的指前因子,测得在相同温度下升高20K时,反应(1)和反应(2)的反应速率分别提高2倍和3倍,说明反应(1)的活化能En,1()反应(2)的活化能En,2,而且在同一温度下,反应(1)的k1()反应(2)的k2.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应(1)和反应(2)具有相同的指前因子,测得在相同温度…”相关的问题
更多“已知反应(1)和反应(2)具有相同的指前因子,测得在相同温度…”相关的问题
有相同物质的量浓度的A,B、C、D四种一元酸的溶液.已知: (1)A溶液的pH大于8溶液; (2)B的钠盐溶液的碱性大于同浓度的C的钠盐溶液; (3)A溶液与锌反应的速率大于D溶液与锌反应的速率. 则这四种酸的酸性从强到弱的顺序是____________________.
已知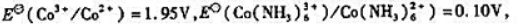
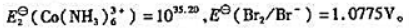
(1)计算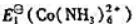 ;
;
(2)写出[Co(NH3)6]2+与Br2(l)反应的离子方程式,计算25℃时该反应的标准平衡常数.
已知下列两个反应:
(1)2H2(g)+O2(g)=2H2O(1);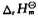 (298K)=-571.70kJ·mol-1
(298K)=-571.70kJ·mol-1
(2)2H2(g)+O2(g)=2H2O(g);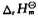 (298K)=-483.65kJ· mol-1
(298K)=-483.65kJ· mol-1
求298K时水的标准摩尔汽化热。
已知ϕθ(Cu2+/Cu+)=0.153V,ϕθ(I2/I-)=0.536V.
(1)计算ϕθ(Cu2+/CuI)的值.
(2)计算当c(Cu2+)=0.50mol·L-1,c(I-)=0.10mol·L-1时,反应2Cu2++4I-=2Cul+I2的标准平衡常数Kθ.
(3)判断在条件(2)下该反应的自发进行方向.[已知Kspθ(CuI)=1.27X10-12]
已知电对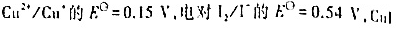 的
的
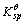 =1.3×10-12。
=1.3×10-12。
(1)试求氧化还原反应
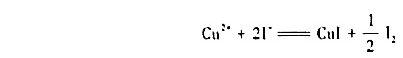
298K时的平衡常数;
(2)若溶液中Cu2+的起始浓度为0.10 mol·dm-3,I-的起始浓度为1.0 mol·dm-3,试计算达到平街时留在溶液中Cu2+的浓度。
某温度下,反应A2+B2 2AB在密闭容器中进行,平衡后各物质的浓度分别为:c(A2)=0.33mol·L-1,c(B2)=3.33mol·L-1,c(AB)=0.67mol·L-1。求:(1)此温度下达到平衡时的平衡常数
2AB在密闭容器中进行,平衡后各物质的浓度分别为:c(A2)=0.33mol·L-1,c(B2)=3.33mol·L-1,c(AB)=0.67mol·L-1。求:(1)此温度下达到平衡时的平衡常数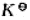 ;(2)反应物的初始浓度;(3)A2的转化率(是指平衡时已转化了的某反应物的量与转化前该反应物的量之比)是多少?
;(2)反应物的初始浓度;(3)A2的转化率(是指平衡时已转化了的某反应物的量与转化前该反应物的量之比)是多少?
体积为1dm3的抽空密闭容器中放有0.03458molN2O4(g),发生如下分解反应:

50℃时分解反应的平衡总压为130.0kPa.已知25℃时N2O4(g)和NO2(g)的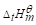
分别为9.16kJ·mol-1和33.18kJ·mol-1.设反应的ΔTGp,m=0.
(1)计算50℃时N2O4(g)的解离度及分解反应的Kθ;
(2)计算100C时反应的Kθ.
反应按下式进行:2NO+2H3=2H2O+N2实验测得下列数据:

(1)求该反应的速率方程式。
(2)求反应级数
(3)求反应速率常数。
A.2:3
B.3:2
C.1:2
D.1:1
(1)写出H2(g),CO(g),CH3OH(I)燃烧反应的热化学方程式;
(2)甲醉的合成反应为:CO(g)+2H2(g)→CH3OH(l).
利用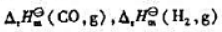
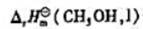 计算该反应的
计算该反应的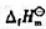 .
.