 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
无色晶体A易溶于水。将A在煤气灯上加热得到黄色固体B和棕色气体C。B溶于硝酸后又得A水溶液。碱性条件下A与次氯
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“无色晶体A易溶于水。将A在煤气灯上加热得到黄色固体B和棕色气…”相关的问题
更多“无色晶体A易溶于水。将A在煤气灯上加热得到黄色固体B和棕色气…”相关的问题
共热得黄绿色气体(D)和近乎无色溶液(E)。将溶液(E)和溶液(C)混合能生成沉淀(B)。将气体(D)通入(A)的溶液中可得(C)。试给出(A),(B),(C),(D)和(E)所代表的物质的化学式,并用化学反应方程式表示各过程。
芒硝化学式为Na2SO4·10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物。用如图所示装置电解硫酸钠溶液,模拟工业上离子交换膜法制烧碱的方法。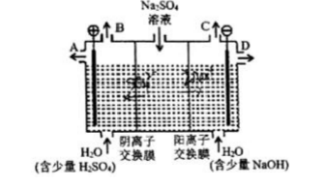 (1)该电解槽的阴极反应式为()。
(1)该电解槽的阴极反应式为()。
(2)电解时,通过阴离子交换膜的离子数()通过阳离子交换膜的离子数。(填大于、小于或等于)。
(3)制得的氢氧化钠溶液从出口()(填写“A”、“B”、“C”、“D”)导出。
(4)①若将制得的氧气、氢氧化钠溶液与天然气组合为甲烷燃料电池,则电池负极的电极反应式为()。
②若将该电池连接两惰性电极,用于电解800mLlmol/L的AgNO3溶液,当原电池中消耗CH4的体积在标况下为0.224L时,电解池中阴极将得到()g的单质,电解池中H+的浓度为()(假设溶液体积不变)。
推理判断:
(1)无色晶体(A)在电炉高温下与碳反应得到灰黑色单质(B),(B)与浓氢氧化钠溶液共热生成无色气体(C)和物质(D)的溶液。气体(C)可以使灼热的黑色氧化铜变成单质铜。(A)与氢氟酸作用有气体(E)生成,(E)通水中生成白色沉淀(F)和气体(G),(G)与过量反应物(E)化合得(H)的溶液。(H)的溶液与过量氯化钾作用可以结晶出(1)。(A)与碳酸钠共熔生成物质(D),(A)与炭粉共热的体系通氧气有无色液体(J)生成,(J)与水反应可得(F)。
试给出(A),(B),(C),(D),(E),(F),(G),(H),(I)和(J)的化学式,并完成各步的化学反应方程式。
(2)蓝黑色化合物(A)不溶于水,但可溶于稀盐酸生成(B)的溶液,稀释该溶液时,析出白色沉淀(C),酸化时.沉淀溶解。向(B)的溶液中通硫化氢时,生成灰黑色沉淀(D),该沉淀可溶于浓盐酸。(D)与硝酸反应时产生浅黄色沉淀(E),无色气体(F)和化合物(C)的溶液。(F)在空气中迅速变成红棕色。向(G)的溶液中通硫化氢时,生成黄色沉淀(H)。
试给出(A),(B),(C),(D),(E),(F),(G)和(H)的化学式,并完成各步的化学反应方程式。
(3)金属单质(A)与氯气在加热时反应生成无色液体(B),(B)经金属(A)处理转变为固体化合物(C)。向(C)的盐酸溶液中通入硫化氢气体生成灰黑色沉淀(D),(D)不溶于硫化钠溶液,但可溶于过硫化钠溶液形成(E)的溶液。向(E)的溶液中加入盐酸生成黄色沉淀(F),并有气体(G)放出。
试给出(A),(B),(C),(D),(E),(F)和(G)的化学式,并完成各步的化学反应方程式。
(4)红色化合物(A)经稀硝酸处理后得到黑色沉淀物(B)和无色透明溶液,从该溶液中可以结晶出无色品体(C)。晶体(C)加热时放出红棕色气体(D)。(B)在酸性介质中与二价锰离子作用,溶液逐渐变为紫红色,说明有化合物(E)生成。若向(C)的水溶液中滴稀盐酸有白色沉淀(F)生成,(F)不溶于氨水;若向(C)的水溶液中滴碘化钾溶液,则生成黄色沉淀(G);若向(C)的水溶液中滴加氢氧化钠溶液,有白色沉淀(H)生成,氢氧化钠过量则沉淀消失。
试给出(A),(B),(C),(D),(E),(F),(G)和(H)的化学式,并完成各步的化学反应方程式。
(5)物质(A)为黄灰色固体,与水反应得白色沉淀(B)、气体(C)及无色溶液。(B)可以溶于氢氧化钠溶液,若与氧化物(D)作用将生成(E)和水。(B)受热脱水生成(F),经过高温灼烧的(F)既不溶于酸,也不溶于碱,但与焦硫酸钾共熔可得两种能溶于水的化合物,其中一种是(E)。将气体(C)通入硝酸铅溶液得黑色沉淀(G),(G)与臭氧反应转化为白色固体(H)。
试给出(A),(B),(C),(D),(E),(F),(G)和(H)的化学式,并完成各步的化学反应方程式。
A.温度和溶剂种类对NaOH的溶觯度都有影响
B.NaOH易溶于水,也易溶于酒精
C.40℃,40 gNaOH溶解在l00 g酒精中达到饱和
D.将等质量40℃的饱和NaOH水溶液和饱和NaOH酒精溶液降温至20C,析出的晶体前者比后者多
A.分子晶体
B.离子晶体
C.原子晶体
D.金属晶体