 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度分别为0.1、0.2、0和平衡浓度分别为0.05、0.05、0.1mol·L-1下列说法错误的是()
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y⇌2Z,其平衡常数为1 600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
 答案
答案
C、增大压强使平衡向生成Z的方向移动,平衡常数增大
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y⇌2Z,其平衡常数为1 600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
 答案
答案
C、增大压强使平衡向生成Z的方向移动,平衡常数增大
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度分别为0…”相关的问题
更多“在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度分别为0…”相关的问题
A.v(X)= 0.10 mol / (L•min)
B.Y的转化率为25%
C.反应物总能量大于生成物总能量
D.平衡时,c(X):c(Y):c(Z)=1:3:2
A.x+y<z
B.平衡向正反应方向移动
C.的转化率增大
D.的体积分数下降
A.1
B.2
C.3
D.4
A.4
B.3
C.2
D.1
A.Z为0.3 mol•L-1
B.Y2为0.4 mol•L-1
C.X2为0.2 mol•L-1
D.Z为0.4 mol•L-1
A.X>Y>Z
B.X>Z>Y
C.Y>X>Z
D.无法比较
g)和H2O(l)。过程放热401.727kJ。求
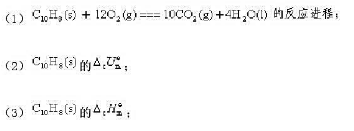
A.Y、Z、X
B.X、Y、Z
C.X、Z、Y
D.Z、Y、X
体积为1dm3的抽空密闭容器中放有0.03458molN2O4(g),发生如下分解反应:

50℃时分解反应的平衡总压为130.0kPa.已知25℃时N2O4(g)和NO2(g)的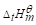
分别为9.16kJ·mol-1和33.18kJ·mol-1.设反应的ΔTGp,m=0.
(1)计算50℃时N2O4(g)的解离度及分解反应的Kθ;
(2)计算100C时反应的Kθ.