 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有机物在CO2气流下通过氧化剂及金属铜燃烧管分解,其中氮元素转化成()气体。
A、N2
B、N2O
C、NO
D、NO2
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、N2
B、N2O
C、NO
D、NO2
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“有机物在CO2气流下通过氧化剂及金属铜燃烧管分解,其中氮元素…”相关的问题
更多“有机物在CO2气流下通过氧化剂及金属铜燃烧管分解,其中氮元素…”相关的问题
A.C4H12O2
B.C3H8O
C.C2H6O
D.C2H4
A.除去CO2中混有少量的CO:导出点燃
B.粗盐提纯的步骤:溶解→过滤→蒸发→冷却结晶→过滤
C.除去H2中混有的HCl:将气体通过装有NaOH溶液的洗气瓶
D.除去铜粉中混有的CuO:用足量的稀硫酸浸泡后过滤、洗涤
A.铁能将铜从硫酸铜溶液中置换出来——金属活动性顺序铁在铜之前
B.铝制品抗腐蚀能力比铁制品强——金属活动性顺序铝在铁之前
C.在铁制品表面涂油漆——通过隔绝空气与水防止铁生锈
D.钢可以制作坦克装甲车——合金具有硬度大、韧性好的优点
A.货物具有较大危急性、包装强度要求高
B.货物具有较大危急性、包装强度要求较高
C.货物具有中等危急性、包装强度要求高
D.货物具有中等危急性、包装强度要求较高
某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾其设计的实验过程为:
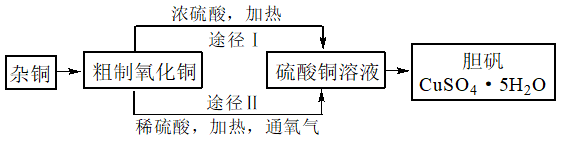
问题一、杂铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将铜粉置于()内(用以下所给仪器的编号填入,下同),取用该仪器应使用(),灼烧完成后该仪器应放在()上冷却,不能直接放在桌面上。
所用仪器:
a蒸发皿
b坩埚
c石棉网
d外表皿
e坩埚钳
f试管夹
问题二、杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物,用以制取胆矾。灼烧后含有少量铜的可能原因是()。
a灼烧过程中部分氧化铜被复原
b灼烧不充分铜未被完全氧化
c氧化铜在加热过程中分解生成铜
d该条件下铜无法被氧气氧化
问题三、通过途径II实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、()、()、冷却结晶、()、自然干燥。
问题四、由粗制氧化铜通过两种途径制取胆矾,与途径I相比,途径II有明显的两个优点是:()、()。
问题五、途径II反应的化学方程式为:()。
A.工频参考电流下的工频参考电压
B.直流1mA电压(U1mA)及在075U1mA下漏电流测量
C.运行中持续电流检测
D.放电计数器功能检查
A.排水法收集O2:导气管口刚有气泡冒出立即收集,收集到的O2更纯净
B.除粗盐中难溶性杂质:将粗盐加入足量水中充分溶解后过滤,避免产率偏低
C.测定空气里O2含量:点燃红磷慢慢伸入集气瓶并塞紧瓶塞,导致测定结果偏低
D.探究CO2性质:将CO2快速倒入盛有燃着蜡烛的烧杯中,便于观察低处蜡烛先熄灭