 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
十二水合硫酸铝钾[KAI(SO4)2・12H2O]俗名明矾,在生活、医药、工业上应用广泛。下面是实脸室探究从铝土矿(主要成分是氧化铝,含少量氧化铁和二氧化硅杂质)制备明矾的流程示意图。![十二水合硫酸铝钾[KAI(SO4)2・12H2O]俗名明矾,在生活、医药、工业上应用广泛。下面是实脸](https://img2.soutiyun.com/shangxueba/askkp/2022-12/22/484/20221222202922290.png) 已知:二氧化硅不溶于水,也不与硫酸反应。(1)铝元素在地壳中以()态存在,写出KAl(SO4)·12H2O溶于水的电离方程式()。当明矾溶液中混有NaCl时,简述如何检验Cl()。(2)滤渣1主要为()(填化学式);以Al2O3为原料,制备该单质铝的反应方程式()。(3)若A为金属单质,则滤渣2的成分有()。(4)操作1是蒸发溶剂至有大量晶膜、冷却结晶。实验室进行该操作时,需要的实验仪器有铁架台、()。(5)如图为某硫酸试剂瓶的标签。若用其配制100mL3mol/L的溶液,需该硫酸()mL(含ρ的表达式)。若此硫酸物质的量浓度为c1,35%的硫酸物质的浓度为c2,则c1()2c2(填大于,小于或等于)。
已知:二氧化硅不溶于水,也不与硫酸反应。(1)铝元素在地壳中以()态存在,写出KAl(SO4)·12H2O溶于水的电离方程式()。当明矾溶液中混有NaCl时,简述如何检验Cl()。(2)滤渣1主要为()(填化学式);以Al2O3为原料,制备该单质铝的反应方程式()。(3)若A为金属单质,则滤渣2的成分有()。(4)操作1是蒸发溶剂至有大量晶膜、冷却结晶。实验室进行该操作时,需要的实验仪器有铁架台、()。(5)如图为某硫酸试剂瓶的标签。若用其配制100mL3mol/L的溶液,需该硫酸()mL(含ρ的表达式)。若此硫酸物质的量浓度为c1,35%的硫酸物质的浓度为c2,则c1()2c2(填大于,小于或等于)。![十二水合硫酸铝钾[KAI(SO4)2・12H2O]俗名明矾,在生活、医药、工业上应用广泛。下面是实脸](https://img2.soutiyun.com/shangxueba/askkp/2022-12/22/752/20221222202902517.png) (6)工业生产中,获取明矾晶体后的母液应该()(填序号)。A、弃去B、返回酸浸流程重复利用C、返回滤液1重复利用D、返回滤液2重复利用
(6)工业生产中,获取明矾晶体后的母液应该()(填序号)。A、弃去B、返回酸浸流程重复利用C、返回滤液1重复利用D、返回滤液2重复利用
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“十二水合硫酸铝钾[KAI(SO4)2・12H2O]俗名明矾,…”相关的问题
更多“十二水合硫酸铝钾[KAI(SO4)2・12H2O]俗名明矾,…”相关的问题
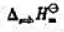 =180.0kJ·mol-1,第一、第二电离能分别为
=180.0kJ·mol-1,第一、第二电离能分别为















