题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知一试样为可能含有Na3PO4,NaH2PO4,Na2HPO4的混合物,同时含有惰性杂质。取此试样2.00g,用甲基红作指示剂,
已知一试样为可能含有Na3PO4,NaH2PO4,Na2HPO4的混合物,同时含有惰性杂质。取此试样2.00g,用甲基红作指示剂,以0.500mol/L的HCl溶液滴定时,需要32.0mL滴定至终点。同样重量的该试样,用酚酞作指示剂时,需要用0.500mol/L的HCl溶液12.0mL滴定至终点。求试样中各组分和惰性杂质的质量分数。(MNa3PO4=163.94,MNa2HPO4=141.94,MNaH2PO4=119.94)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“已知一试样为可能含有Na3PO4,NaH2PO4,Na2HP…”相关的问题
更多“已知一试样为可能含有Na3PO4,NaH2PO4,Na2HP…”相关的问题
 2)对于原料ALCL3的制取,某兴趣小组设计了如下装置:
2)对于原料ALCL3的制取,某兴趣小组设计了如下装置: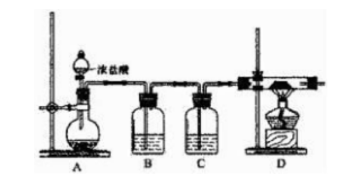 ①连接好装置后,应进行的第一步操作是();为保证产物的纯净,应待D中()(填现象)再加热酒精灯。
①连接好装置后,应进行的第一步操作是();为保证产物的纯净,应待D中()(填现象)再加热酒精灯。