 更多“已知CO在催化剂活性中心的吸附速率比H2快,生产上应采用()…”相关的问题
更多“已知CO在催化剂活性中心的吸附速率比H2快,生产上应采用()…”相关的问题
第4题
已知下列冶炼条件:焦比460kg/t,煤比80kg/t,炉尘12kg/t,f=12g/m3;含碳量为:焦炭85%,煤65%,炉尘3%,生铁4.2%;煤气成分:CO:22%,CO2∶18.2%,CH4∶0.8%,H2;0.4%,N2∶58.6%,不计焦炭和煤粉挥发份的影响,求风量、炉顶煤气量和炉缸煤气量。
第5题
已知反应CO2(g)+H2(g)=CO(g)+H2O(g)在973K时的=0.618.若系统中各组分气体分压为p
已知反应CO2(g)+H2(g)=CO(g)+H2O(g)在973K时的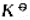 =0.618.若系统中各组分气体分压为p(CO2)=p(H2)=127kPa,p(CO)=p(H2O)=76kPa,计算此时
=0.618.若系统中各组分气体分压为p(CO2)=p(H2)=127kPa,p(CO)=p(H2O)=76kPa,计算此时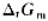 (973K)时值并判断反应进行的方向。
(973K)时值并判断反应进行的方向。
第7题
已知298.15K时化学反应在催化剂的作用下反应速率大大加快时,反应的(298.15K)=().
已知298.15K时化学反应在催化剂的作用下反应速率大大加快时,反应的(298.15K)=().
点击查看答案
已知298.15K时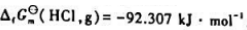 化学反应
化学反应
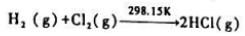
在催化剂的作用下反应速率大大加快时,反应的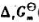 (298.15K)=().
(298.15K)=().
第9题
有关一氧化碳加氢合成甲醇反应条件叙述正确的是()。
A.升高温度,反应速度增加
B.升高温度,平衡常数下降
C.增加压力,提高甲醇的平衡产率
D.原料气H2:CO的理论比3∶1
E.适当的空速可提高生产能力,减少副反应
第10题
已知反应在催化剂H+存在且c(CH3COCH3)>>c(I2)时,反应速率不随c(I2)变
A.v=kc2(CH3COCH3)c(H+)
B.v=kc(CH3COCH3)c(H+)
C.v=kc(CH3COCH3)c(l2)
D.v=kc(CH3COCH3)c2(l2)
第11题
CO与Hb结合速率为O2与Hb结合速度的____________,但HbCO的解离速度为HbO2解离速度___________,
因此CO与Hb的亲和力比O2大___________。
点击查看答案


 如果结果不匹配,请
如果结果不匹配,请 
















