 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
铅(Pb)的原子序数为82,有+2、+4两种常见化合价。PbO2随温度的升高发生如下变化:PbO2→Pb2O3→Pb3O4→PbO。下列说法不正确的是()
A.Pb位于周期表ⅣA族
B.Pb3O4可以写成2PbO·PbO2
C.PbO2分解生成Pb2O3同时生成O2
D.PbO2可作为铅蓄电池的正极,放电时发生氧化反应
 答案
答案
D、PbO2可作为铅蓄电池的正极,放电时发生氧化反应
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Pb位于周期表ⅣA族
B.Pb3O4可以写成2PbO·PbO2
C.PbO2分解生成Pb2O3同时生成O2
D.PbO2可作为铅蓄电池的正极,放电时发生氧化反应
 答案
答案
D、PbO2可作为铅蓄电池的正极,放电时发生氧化反应
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“铅(Pb)的原子序数为82,有+2、+4两种常见化合价。Pb…”相关的问题
更多“铅(Pb)的原子序数为82,有+2、+4两种常见化合价。Pb…”相关的问题
工业上利用铅浮渣(主要成分是PbO,Pb,含有少量Ag,CaO和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示: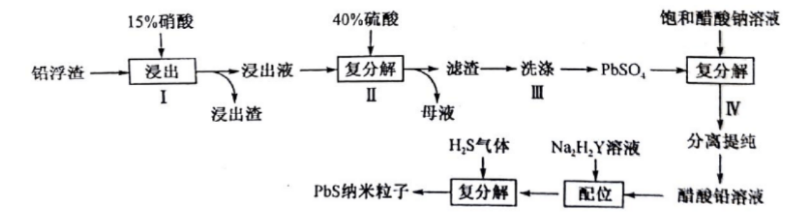 已知:25℃时,
已知:25℃时,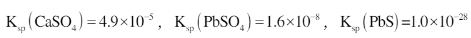 (1)步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有()。
(1)步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有()。
(2)写出Pb参加反应的化学方程式:()。保持铅剩余的原因是()。
(3)母液的主要成分是()(写化学式),可以循环利用。若母液中残留的SO42-过多,循环利用时可能出现的问题是()。
(4)若浸出液中c(Ca=2+)=0.05mol.L-1,步骤Ⅱ当pb2+完全沉淀后滤渣中是否有CaSO4存在?()(填有或没有)理由是()(通过计算说明)。
A、1
B、2
C、4
D、8
设某经济只有a、b两个市场。a市场的需求和供给函数为Qda=13-2Pa+Pb、Qsb=-4+2Pa,b市场的需求和供给函数为Qdb=20+Pa-Pb、Qsb=-5+4Pb。试确定:
(1)当Pb=1时,a市场的局部均衡;
(2)当Pa=1时,b市场的局部均衡;
(3)(Pa=1,Pb=1)是否代表一般均衡?
(4)(Pa=5,Pb=3)是否是一般均衡价格?
(5)一般均衡价格和一般均衡产量为多少?
A.对于核素发出的γ射线,其穿透力强,需要选用原子序数高的强衰减材料如铅和混凝土做屏蔽体材料
B.对于发射β-粒子的放射性核素,应当用低原子序数的材料如铝和塑料作盛源容器
C.对于发射β+粒子的放射性核素,应当采用原子序数高的强衰减材料如铅和混凝土做屏蔽体材料
D.对于发射a粒子的核素,因为能量高,应当采用原子序数高的强衰减材料如铅和混凝土做屏蔽体材料
解释实验现象:
(1)将CO气体通入二氯化钯溶液中,溶液变黑。
(2)将甲硅烷通入KMnO4溶液中,溶液褪色,有棕黑色沉淀和气泡产生。
(3)将CO2气体通入澄清的石灰水中,溶液变浑浊,继续通入至过量后,溶液又变澄清。
(4)Al4C3和水作用有白色沉淀和气体生成。
(5)向SnCl4溶液中滴加Na2S溶液,有沉淀生成,继续加入沉淀又溶解,再以稀盐酸处理此溶液,又析出沉淀。
(6)向氯化汞溶液中滴加SnCl2溶液,先生成白色沉淀,随着SnCl2溶液滴入至过量,沉淀逐渐变灰、变黑。
(7)向Pb(NO3)2溶液中滴加K2CrO4的中性或弱碱性溶液,生成黄色沉淀;而向Pb(NO3)2溶液中滴加K2CrO4的酸性或强碱性溶液,则无沉淀生成。