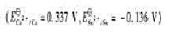题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
浓度均为20*10-2mol·L-1的Th4+, La3+混合溶液,欲用0.02000mol·L

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“浓度均为20*10-2mol·L-1的Th4+, La3+混…”相关的问题
更多“浓度均为20*10-2mol·L-1的Th4+, La3+混…”相关的问题
若溶液中Fe2+、Al3+浓度均为0.01mol·L-1,能否控制酸度,用EDTA选择滴定Fe2+?如何控制溶液酸度。
含H2SO4(Mr=98.07)和H3PO4(Mr=98.00)的混合液两份(体积均为25.00mL),分别用0.1018mol·L-1的NaOH标准溶液滴定。第一份以甲基橙(pKHn=3.4)作指示剂,需25.18mL 滴至终点;第二份以酚酞(pKHn=9.1)作指示剂,需35.22mL到达终点。试求混合液中每种酸的浓度?(已知H3PO4的Ka1=10-2.12,Ka2=10-7.21,Ka3=10-12.7)
A.1.0×10-4mol·L-1
B.1.0×10-7mol·L-1
C.0.10mol·L-1
D.1.0X10-12mol·L-1
某温度下,反应A2+B2 2AB在密闭容器中进行,平衡后各物质的浓度分别为:c(A2)=0.33mol·L-1,c(B2)=3.33mol·L-1,c(AB)=0.67mol·L-1。求:(1)此温度下达到平衡时的平衡常数
2AB在密闭容器中进行,平衡后各物质的浓度分别为:c(A2)=0.33mol·L-1,c(B2)=3.33mol·L-1,c(AB)=0.67mol·L-1。求:(1)此温度下达到平衡时的平衡常数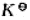 ;(2)反应物的初始浓度;(3)A2的转化率(是指平衡时已转化了的某反应物的量与转化前该反应物的量之比)是多少?
;(2)反应物的初始浓度;(3)A2的转化率(是指平衡时已转化了的某反应物的量与转化前该反应物的量之比)是多少?
(1)每升碱液吸收了多少克CO2?
(2)用该碱液滴定某一元弱酸,若浓度仍以0.1026ml·L-1计算,会引起多大误差?
用惰性电极电解下列电解质溶液(浓度均为0.1 mol/L),电解片刻后溶液pH明显增大的是__________ (填序号)。
①Na2SO4溶液
②稀H2SO4溶液
③NaCl溶液
电解Cu2+和Sn2+的混合酸性溶液,Cu2+和Sn2+的浓度均为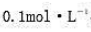 ,以铂为电极进行电解。
,以铂为电极进行电解。
(1)在阴极上何种离子先析出?
(2)若要使两种金属离子完全分开,阴极电位应控制多少?