题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
一种新型燃料电池,是用两根金属铂做电极插入KOH溶液中,然后向两极上分别通入CH3OH和O2,下解说法不正确的是()
A.通入CH3OH的电极为负极
B.随着放电的进行,负极附近pH上升
C.每消耗1mol CH3OH可以向外电路提供6mol e﹣
D.通入O2的一极电极反应为4H2O+2O2﹣+8e﹣═8OH﹣
 答案
答案
B、随着放电的进行,负极附近pH上升
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.通入CH3OH的电极为负极
B.随着放电的进行,负极附近pH上升
C.每消耗1mol CH3OH可以向外电路提供6mol e﹣
D.通入O2的一极电极反应为4H2O+2O2﹣+8e﹣═8OH﹣
 答案
答案
B、随着放电的进行,负极附近pH上升
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“一种新型燃料电池,是用两根金属铂做电极插入KOH溶液中,然后…”相关的问题
更多“一种新型燃料电池,是用两根金属铂做电极插入KOH溶液中,然后…”相关的问题
A.通CO的一极是电池的正极
B.负极发生的电极反应是O2+2CO2+4e-=2CO32-
C.负极发生的电极反应是CO+CO32--2e-=2CO2
D.正极发生氧化反应
A.阴阳两极都用石墨
B.铜作阳极铁作阴极
C.铁作阳极铜作阴极
D.铜作阳极铂作阴极
过度排放CO2会造成”温室效应“,科学家正在研究如何将CO2转化为可以利用的资源,其中一种方案就是将CO2转化为可再生燃料甲醇(CH3OH)。其化学方程式为: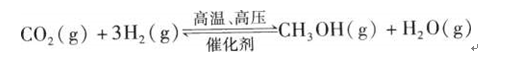
请填空:
问题一、写出上述反应的平衡常数表达式K=()。
问题二、在容积为2L的密闭容器中,用一定量二氧化碳与一定量氢气在一定条件下合成甲醇,实验结果如下图。以下说法正确的选项是()。
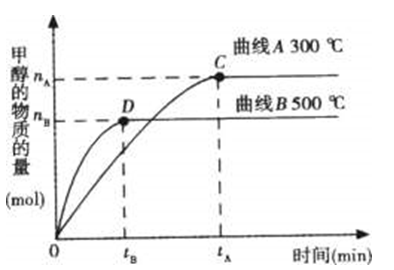
A在300℃,从反应开始到平衡,甲醇的平均反应速率
B反应体系从300℃升温到500℃,平衡常数K变大
C该反应的正反应为放热反应
D处于C点的反应体系从300℃升温到500℃n(H2)/n(CH3OH)增大
问题三、25℃、1.01×105Pa时16g液态甲醇完全燃烧,当恢复至原状态时,放出362.9kJ热量,此反应的热化学方程式为()。
问题四、选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此燃料电池负极应加入或通入的物质是,正极的电极反应式为()。
从铝+矿(主要成分是Al2O3,含RO2、Fe2O3等杂质)中提取Al2O3的一种工艺流程如图13所示: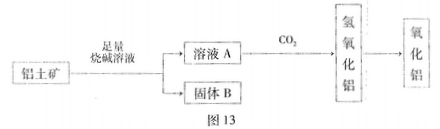
问题一、元素R位于周期表中的第三周期,其最高正化合价和负化合价的绝对值相等。RO2的用途有(写出1条即可)()。
问题二、铝土矿加入足量烧碱溶液后主要反应的离子方程式为
①()。
②()。
问题三、工业上通过电解氧化铝和冰晶石的熔融液来冶炼金属铝。已知电极材料为惰性材料,阳极反应式为()。
问题四、氧化铝与焦炭的混合物在氮气中高温加热反应,制得新型非金属材料AIN与一种中学常见气体X。已知每转移3mole-,有1.5mol化合物X生成,此反应的化学方程式()。
近年来AIST报告正在研制一种“高容量、低成本”的锂—铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH一,下列说法不正确的是()。
A.放电时,Li+透过固体电解质向Cu极移
B.放电时,正极的电极反应式为O2+2H2O+4e一=4OH—
C.通空气时,铜被腐蚀,表面产生Cu2O
D.通空气时,整个反应过程中,铜相当于是催化剂
电解Cu2+和Sn2+的混合酸性溶液,Cu2+和Sn2+的浓度均为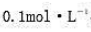 ,以铂为电极进行电解。
,以铂为电极进行电解。
(1)在阴极上何种离子先析出?
(2)若要使两种金属离子完全分开,阴极电位应控制多少?