 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列有机物滴入NaOH溶液中会出现分层现象,然后用水浴加热,分层现象逐渐消失的是()
A.乙酸
B.苯酚溶液
C.己烯
D.乙酸乙酯
 答案
答案
D、乙酸乙酯
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.乙酸
B.苯酚溶液
C.己烯
D.乙酸乙酯
 答案
答案
D、乙酸乙酯
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列有机物滴入NaOH溶液中会出现分层现象,然后用水浴加热,…”相关的问题
更多“下列有机物滴入NaOH溶液中会出现分层现象,然后用水浴加热,…”相关的问题
A.CO2通入NaAlO2溶液中AlO+CO2+H2O===Al(OH)3↓+CO
B.Al2O3与过量氨水Al2O3+6NH3•H2O===2Al3++6NH
C.向AlCl3溶液中加入过量NaOH溶液Al3++3OH-===Al(OH)3↓
D.向AlCl3溶液中滴入过量的氨水Al3++3NH3•H2O===Al(OH)3↓+3NH
将含有0.1 mol AlCl3的溶液,逐滴加入4 mol/L的NaOH溶液,如果出现3.9 g A1(OH)3沉淀,则加入的NaOH溶液的体积为__________mL或__________mL。
以黄铁矿为原料制硫酸产生的废渣中含Fe2O3、SiO2、Al2O3、CaO、MgO等。现以此废渣制备铁红(Fe2O3)的过程如下。此浓度时,部分阳离子以氢氧化物形式沉淀时溶液的pH由见右表。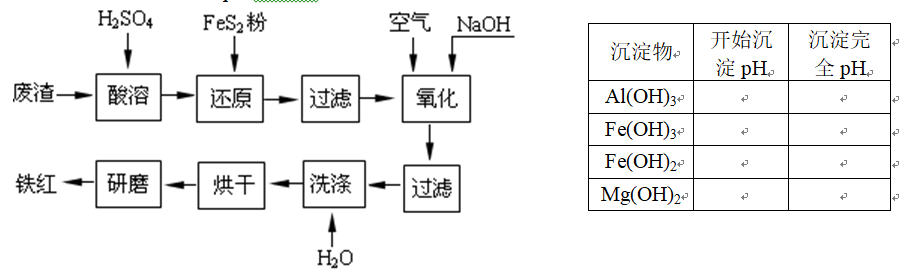 问题一、酸溶过程中Fe2O3与稀硫酸反应的化学方程式是()。
问题一、酸溶过程中Fe2O3与稀硫酸反应的化学方程式是()。
问题二、复原过程中加入FeS2是将溶液中的Fe3+复原为Fe2+,而本身被氧化为SO42-,写出有关的离子方程式:()。
问题三、氧化过程中通入空气和加入NaOH是为了将溶液中的铁元素充分转化为沉淀而析出,写出有关的离子方程式:()。
问题四、为了确保铁红的质量,氧化过程需要调节溶液pH的范围为()≤pH<()。
问题五、假设NaOH加入过量,所的铁红产品中有其它杂质,但可能无Al2O3,其原因是(用离子方程式表示):() 。
A.将少量氨水滴入硫酸铝溶液中,搅拌
B.将少量氢氧化钠溶液滴入硫酸铝溶液中,搅拌
C.将少量硫酸铝溶液滴入氢氧化钠溶液中,搅拌
D.将少量硫酸铝溶液滴入氨水中,搅拌