 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将标准状况下的2.24L CO2通入150mL 1mol/LNaOH溶液中,下列说法正确的是()
A.(HCO3-)略大于c(CO32—)
B.能使酸性高锰酸钾溶液褪色
C.(Na+)等于c(CO32—)与c(HCO3—)之和
D.(HCO3—)略小于c(CO32—)
 答案
答案
A、(HCO3-)略大于c(CO32—)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.(HCO3-)略大于c(CO32—)
B.能使酸性高锰酸钾溶液褪色
C.(Na+)等于c(CO32—)与c(HCO3—)之和
D.(HCO3—)略小于c(CO32—)
 答案
答案
A、(HCO3-)略大于c(CO32—)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“将标准状况下的2.24L CO2通入150mL 1mol/L…”相关的问题
更多“将标准状况下的2.24L CO2通入150mL 1mol/L…”相关的问题
A.
CO2通入可溶性硅酸盐中析出硅酸沉淀
B.
CO2溶于水形成碳酸,SiO2难溶于水
C.
高温下SiO2与碳酸盐反应生成CO2
D.在可溶性硅酸盐中加盐酸会析出硅酸沉淀
共热得黄绿色气体(D)和近乎无色溶液(E)。将溶液(E)和溶液(C)混合能生成沉淀(B)。将气体(D)通入(A)的溶液中可得(C)。试给出(A),(B),(C),(D)和(E)所代表的物质的化学式,并用化学反应方程式表示各过程。
A.0. 1 mol・L-1NaOH溶液中含有0. 1 mol Na+
B.22 g CO2物质的量为0. 5 mol
C.1 mol Cl2中含有的氯原子数约为6. 02×1023
D.标准状况下,44. 8 L H2O的物质的量为2mol
A.检验溶液中SO42—的方法是:先加入BaCl2溶液,再加盐酸
B.从溴水中提纯单质溴的方法是:先用CCl4萃取,分液后再蒸馏
C.证明气体分子中含有C=C的方法是:将该气体通入KMnO4酸性溶液
D.除去CO2中少量HCl的方法是:将混合气体通过盛有饱和NaHSO3溶液的洗气瓶
解释实验现象:
(1)将CO气体通入二氯化钯溶液中,溶液变黑。
(2)将甲硅烷通入KMnO4溶液中,溶液褪色,有棕黑色沉淀和气泡产生。
(3)将CO2气体通入澄清的石灰水中,溶液变浑浊,继续通入至过量后,溶液又变澄清。
(4)Al4C3和水作用有白色沉淀和气体生成。
(5)向SnCl4溶液中滴加Na2S溶液,有沉淀生成,继续加入沉淀又溶解,再以稀盐酸处理此溶液,又析出沉淀。
(6)向氯化汞溶液中滴加SnCl2溶液,先生成白色沉淀,随着SnCl2溶液滴入至过量,沉淀逐渐变灰、变黑。
(7)向Pb(NO3)2溶液中滴加K2CrO4的中性或弱碱性溶液,生成黄色沉淀;而向Pb(NO3)2溶液中滴加K2CrO4的酸性或强碱性溶液,则无沉淀生成。
A.150mL
B.120mL
C.90mL
D.60mL
生成溶液(D),并放出气体(E),(E)可使红色石蕊试纸变蓝。将CO2气体通入溶液(D)中有白色沉淀(F)生成。试给出(A),(B),(C),(D),(E)和(F)所代表的物质的化学式。
海洋中蕴含丰富的资源,下图涉及多个以海水为原料的生产流程。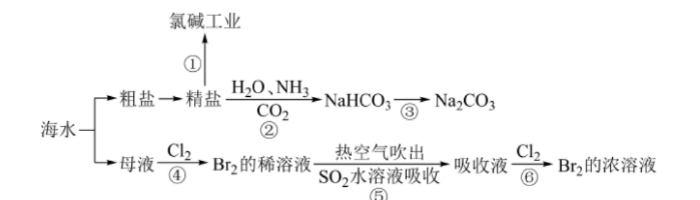 完成下列填空:
完成下列填空:
(1) 步骤①中电解饱和食盐水的化学方程式是()。
(2)工业上用Cl2与KOH(热溶液)制备KClO3,,Cl2+KOH=KCl+KClO3+H2O。配平上述反应方程式,并标出电子转移方向和数目()。
(3)关于卤素的下列说法错误的是()。
A、单质的熔点:Cl2>Br2>I2
B、元素的非金属性:Cl>Br>I
C、单质的氧化性:I2>Br2>Cl2
D、从海洋中获得Cl2,Br2的过程均涉及氧化还原反应
(4)对图中所示生产过程的说法正确的是()。
A、溶解度:NaHCO3>Na2CO3
B、第④⑤⑥步骤中,溴元素均被还原
C、第⑤⑥步骤的目的是进行溴的富集,提高Br2的浓度
D、联碱法与氨碱法相比,NaCl利用率较高,且能耗低
(5)步骤②是在饱和食盐水中先通入NH3再通入CO2,原因是()。
(6)某同学将CO2通入NaOH溶液中,当溶液呈中性时,溶液中浓度最大的微粒是()。
A、c(Na+)B、c(CO32-)C、c(HCO3-)D、c(H+)