 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知某反应在700K时,速率常数为:k=1.2dm3·mol-1·s-1,此反应的活化能为150kJ·mol-1,试计算800K时的反应速率
已知某反应在700K时,速率常数为:k=1.2dm3·mol-1·s-1,此反应的活化能为150kJ·mol-1,试计算800K时的反应速率常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知某反应在700K时,速率常数为:k=1.2dm3·mol-1·s-1,此反应的活化能为150kJ·mol-1,试计算800K时的反应速率常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知某反应在700K时,速率常数为:k=1.2dm3·mol…”相关的问题
更多“已知某反应在700K时,速率常数为:k=1.2dm3·mol…”相关的问题
有双分子反应CO(g)+NO2(g)→CO2(g)+NO(g), e知在540~727 K之间发生定容反应,其速率常数k的表达式为
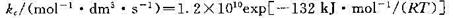
若在600 K时,CO(g )和NO2(g)的初始压力分别为667 Pa和933 Pa.试计算:(1)该反应在600 K时的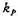 值;(2)反应进行10h后,NO的分压。
值;(2)反应进行10h后,NO的分压。
反应2NO(g)+H2(g)→N2O(g)+ H2O(g)的速率方程为

反应在恒温、恒容的条件下进行,测得实验数据如下:
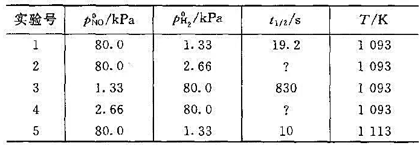
(1)求所缺的半衰期数据;(2)求1093 K时的速率常数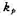 ;(3)求反应的活化能
;(3)求反应的活化能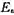 ;(4)提出一个只涉及双分子步骤的反应机理,由此机理可得上述规律;(5)如果1093K时,
;(4)提出一个只涉及双分子步骤的反应机理,由此机理可得上述规律;(5)如果1093K时,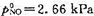 ,
,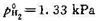 ,求该反应的半衰期。
,求该反应的半衰期。
环丁烯异构化反应是一级反应:
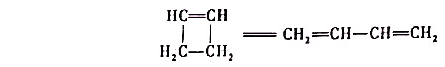
150℃时,速率常数k=2.0×10-4s-1,气态环丁烯的初始浓度为1.89×10-3mol·dm-3,试求:
(1)20min时环丁烯的浓度;
(2)环丁烯的浓度变成1.00×10-3mol·dm-3所需时间。
298 K时,反应N2O4(g)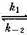 2NO2(g)的速率常数
2NO2(g)的速率常数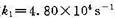 ,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为
,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为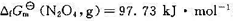 和
和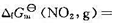 51.25 kJ·mol-1。请计算:(1)在298 K时,N2O4(g)的初始压力为100 kPa,NO2(g)的平衡分压;(2)该反应的弛豫时间r。
51.25 kJ·mol-1。请计算:(1)在298 K时,N2O4(g)的初始压力为100 kPa,NO2(g)的平衡分压;(2)该反应的弛豫时间r。
碘化氢的分解反应为均相二级反应 2HI(g)=H2(g)+I2(g) 已知反应的活化能Ea为185kJ.mol-1,分子的碰撞直径为3.50×10-10m。试确定反应速率常数kHI与温度的关系式并求556K时的反应速率常数。
CSTR中可逆反应的操作状态
在全混流反应器中进行下述可逆反应:

已知正向和逆向反应均为一级,反应速率常数为:k1=8.83×104×exp

(1)该反应是放热反应还是吸热反应?其标准反应热
(2)在340K,A的最大转化率为多少?
(3)在340K,如果停留时间为480s,那么转化率为多少?
(4)如果停留时间保持为480s,请画出在320K至370K之间转化率和温度关系的关系曲线。
(5)如果停留时间为480s,为使A的转化率达到最大值,那么入口温度应为多少?
A.64.81d/(kg。K)
B.64.8J/(kg。K)
C.52.37kJ/kg
D.102.3J/(kg。K)