 更多“一定条件下达到平衡状态的某个反应体系,其总压强必定保持不变(…”相关的问题
更多“一定条件下达到平衡状态的某个反应体系,其总压强必定保持不变(…”相关的问题
A.化学平衡只有在一定的条件下才能保持
B.化学平衡在任何条件下都能保持
C.如果一个可逆反应达到平衡状态后,反应条件改变时,平衡混合物中各组成的百分含量不会改变,从而达到新的平衡状态
D.如果一个可逆反应达到平衡状态后,反应条件改变时,平衡混合物中各组成的百分含量也就随着改变,从而达到新的平衡状态
A.密闭容器中充入1 mol N2和3 mol H2可生成2 mol NH3
B.一定条件下,可逆反应达到平衡状态,该反应就达到了这一条件下的最大限度
C.对于任何反应增大压强,化学反应速率均增大
D.化学平衡是一种动态平衡,条件改变,原平衡状态不会被破坏
过度排放CO2会造成”温室效应“,科学家正在研究如何将CO2转化为可以利用的资源,其中一种方案就是将CO2转化为可再生燃料甲醇(CH3OH)。其化学方程式为: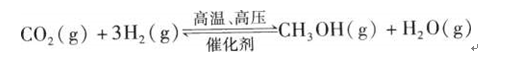
请填空:
问题一、写出上述反应的平衡常数表达式K=()。
问题二、在容积为2L的密闭容器中,用一定量二氧化碳与一定量氢气在一定条件下合成甲醇,实验结果如下图。以下说法正确的选项是()。
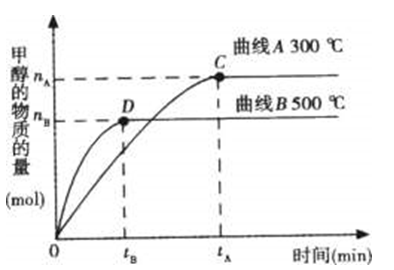
A在300℃,从反应开始到平衡,甲醇的平均反应速率
B反应体系从300℃升温到500℃,平衡常数K变大
C该反应的正反应为放热反应
D处于C点的反应体系从300℃升温到500℃n(H2)/n(CH3OH)增大
问题三、25℃、1.01×105Pa时16g液态甲醇完全燃烧,当恢复至原状态时,放出362.9kJ热量,此反应的热化学方程式为()。
问题四、选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此燃料电池负极应加入或通入的物质是,正极的电极反应式为()。
A.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度
B.当一个可逆反应达到平衡状态时,正反应速率和逆反应速率相等且等于零
C.平衡状态时,各物质的浓度保持相等
D.化学反应的限度不可以通过改变条件而改变
A.平衡右移
B.平衡左移
C.平衡不移动
D.无法判断
A.Z为0.3 mol•L-1
B.Y2为0.4 mol•L-1
C.X2为0.2 mol•L-1
D.Z为0.4 mol•L-1


 如果结果不匹配,请
如果结果不匹配,请 
















