 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在工业生产中为得到质量好、粒度大的晶体,常在介稳区进行结晶。介稳区就是指的()。
A.溶液没有达到饱和的区域
B.溶液刚好达到饱和的区域
C.溶液有一定过饱和度,但程度小,不能自发地析出结晶的区域
D.溶液的过饱和程度大,能自发地析出结晶的区域
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.溶液没有达到饱和的区域
B.溶液刚好达到饱和的区域
C.溶液有一定过饱和度,但程度小,不能自发地析出结晶的区域
D.溶液的过饱和程度大,能自发地析出结晶的区域
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在工业生产中为得到质量好、粒度大的晶体,常在介稳区进行结晶。…”相关的问题
更多“在工业生产中为得到质量好、粒度大的晶体,常在介稳区进行结晶。…”相关的问题
A.蛇纹石质玉和独山玉均属于软玉
B.相同质量级别的钻石,个体愈大愈珍贵
C.翡翠为玉中之王,翡翠的品质决定于它的颜色、透明度(水)和缺隙
D.祖母绿与海蓝宝石的质地,以色正、深艳,透明晶莹,瑕疵少、晶体大的为好
A.适用于一些对振动敏感,易热分解或化学分解,很难以机械研磨方式制细的粉体的制备
B.这种方法已经被用于一些无机物和陶瓷粉体材料的制备
C.合成二氧化硅和a氧化铝时使用的超临界流体是一些超临界温度比较高的溶剂如水、乙醇和戊烷等
D.在超临界水中合成二氧化硅和a氧化铝时操作压力在18-60MPa之间,膨胀前温度300-600度,得到晶体的粒度一般为纳米级
A.73.3 %
B.74.4%
C.75.0%
D.76.8%
氯化镁是重要的无机材料,在常温下易吸湿,可溶于水和乙醇。某兴趣小组以海水为原料制备无水氯化镁。
实验一制备MgCl2·6H2O晶体
以海水为原料,对其进行一系列处理,得到晶体。
(1)除去海水中不溶性杂质常用的实验操作是()(填名称)。
(2)从氯化镁溶液中析出MgCl2·6H2O晶体的结晶方法是()(填“降温结晶”或“蒸发结晶”)。
实验二样品中MgCl2·6H2O晶体含量测定
准确称取实验一制得的MgCl2·6H2O晶体ag于锥形瓶中,加去离子水溶解,依次加入一定量三乙醇胺、NH3-NH4Cl缓冲溶液,摇匀,滴入铬黑T指示剂,用0.02000mol·L-1EDTA(用H2Y2-表示)标准溶液滴定至终点,消耗EDTA溶液的体积VmL。
已知:①0.02000mol·L-1EDTA标准溶液pH约为5,指示剂铬黑T使用的适宜pH范围为8~11,NH3-NH4Cl缓冲溶液pH约为10。
②滴定原理: Mg2++H2Y2-=MgY2-+2H+。
(3)使用的滴定管是()(填“甲”或“乙”)。
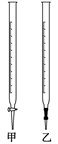 (4)NH3-NH4Cl缓冲溶液的作用是()。
(4)NH3-NH4Cl缓冲溶液的作用是()。
(5)样品中MgCl2·6H2O的质量分数为()。
实验三制备无水氯化镁
利用如图实验装置(夹持和加热装置省略),准确称取一定质量MgCl2·6H2O晶体在HCl气流中小心加热。
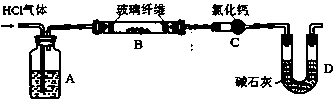 (6)A装置的作用是()。
(6)A装置的作用是()。
(7)某同学在实验前后测得玻璃管B减重m1g,干燥管C增重m2g,m1>m2,其可能的原因是()(用化学方程式表示)。
A.饱和溶液析出晶体后,溶液的溶质质量分数不一定减少
B.河水经过沉降、过滤、活性炭吸附后得到的水是纯净物
C.通过洗洁精的乳化作用,可将食用油溶解于水形成溶液
D.试剂瓶中的溶液在使用时不慎洒出一部分,剩余溶液溶质质量分数减少
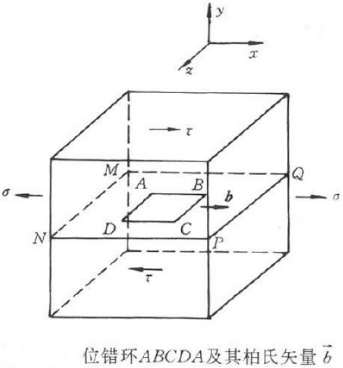
已知位错环ABCDA的柏氏矢量为b,外应力为τ和σ,如图2-3所示。求:
①设想在晶体中怎样才能得到这个位错?
②在足够大的切应力τ作用下,位错环将如何运动?
③在足够大的拉应力σ作用下,位错环将如何运动?
A.工业上常用分离液态空气法制取氧气
B.经过沉淀、过滤后得到的矿泉水是纯净物
C.面粉、煤粉等粉尘遇到明火可能发生爆炸
D.饱和溶液析出晶体后,溶液的溶质质量分数不一定减少