 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于化学反应方向的判断,下列说法中正确的是()
A.温度、压强一定时,放热的熵减小的反应一定能自发进行
B.温度、压强一定时,焓因素和熵因素共同决定一个化学反应的方向
C.反应焓变是决定反应能否自发进行的唯一因素
D.固体的溶解过程与熵变无关
 答案
答案
B、温度、压强一定时,焓因素和熵因素共同决定一个化学反应的方向
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.温度、压强一定时,放热的熵减小的反应一定能自发进行
B.温度、压强一定时,焓因素和熵因素共同决定一个化学反应的方向
C.反应焓变是决定反应能否自发进行的唯一因素
D.固体的溶解过程与熵变无关
 答案
答案
B、温度、压强一定时,焓因素和熵因素共同决定一个化学反应的方向
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对于化学反应方向的判断,下列说法中正确的是()”相关的问题
更多“对于化学反应方向的判断,下列说法中正确的是()”相关的问题
判断下列说法是否正确:
(1)在可逆过程中系统的熵值不变;
(2)如一个化学反应的ΔrH与温度无关,其ΔrS也与温度无关;
(3)根据dG=- SdT+ Vdp,对于任意等温等压过程dT=0, dp=0,则dG 一定为零;
(4)理想气体向真空膨胀△S= nRIn(V1/V2)
(5)在等温情况下,理想气体发生状态变化时,ΔP与ΔG相等;
(6)因为在等温等压下化学反应无论是否可逆,其反应热均等于过程中的SH,所以反应的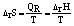
A.对于任何化学反应来说,温度越高,反应速率越大,反应现象就越明显
B.在其他条件不变时,升高温度一定会加快化学反应的反应速率
C.升高温度,放热反应的化学反应速率加快,吸热反应的反应速率变慢
D.降低温度,可能对某些化学反应的速率无影响
A.可逆反应的特征是正反应速率和逆反应速率相等
B.在其它条件不变时,升高温度可以使化学平衡向放热反应的方向移动
C.在其它条件不变时,增大压强一定会破坏气体反应的平衡状态
D.在其它条件不变时,使用催化剂可改变化学反应速率,但不能改变化学平衡状态
A.密闭容器中充入1 mol N2和3 mol H2可生成2 mol NH3
B.一定条件下,可逆反应达到平衡状态,该反应就达到了这一条件下的最大限度
C.对于任何反应增大压强,化学反应速率均增大
D.化学平衡是一种动态平衡,条件改变,原平衡状态不会被破坏
A.ΔrHmθ为H2O(g)的生成热
B.ΔrHmθ为H2(g)的燃烧热
C.ΔrHmθ是负值
D.加压有利于该平衡反应向右进行
A.增加固体碳的物质的量,化学反应速率会加快
B.升高温度,化学反应速率会加快
C.升高温度,化学反应速率会变慢
D.升高温度,固体碳能充分燃烧
A.化学反应中放出的热量与反应物和产物的温度有关
B.在298.15K,0.1013MPa时的反应热称为标准反应热。用△=Hf一表示
C.反应热与反应物和产物的聚集状态无关
D.对同一化学反应,若化学计量方程式的系数不同,反应热的数值也不同
A.物质O催化了物质Z的还原
B.物质R催化了物质Z的还原
C.物质Z催化了物质O的还原
D.物质O催化了物质R的氧化
A.用磁感线可以描述磁场的强弱
B.只要导体在磁场中做切割磁感线运动,该导体中就会产生感应电流
C.通电导体产生的磁场的方向与通过该导体的电流方向有关
D.利用撒在磁体周围的铁屑可以判断该磁体周围各点的磁场方向