 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
配制pH值为5.0的缓冲溶液,需将多少克醋酸钠(CH3COONa·3H2O)溶解于300mL、0.50mol·L-1HAc溶液中(忽略体积变化
配制pH值为5.0的缓冲溶液,需将多少克醋酸钠(CH3COONa·3H2O)溶解于300mL、0.50mol·L-1HAc溶液中(忽略体积变化)?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
配制pH值为5.0的缓冲溶液,需将多少克醋酸钠(CH3COONa·3H2O)溶解于300mL、0.50mol·L-1HAc溶液中(忽略体积变化)?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“配制pH值为5.0的缓冲溶液,需将多少克醋酸钠(CH3COO…”相关的问题
更多“配制pH值为5.0的缓冲溶液,需将多少克醋酸钠(CH3COO…”相关的问题
(1)实际上所配缓冲溶液的pH为多少?
(2)若要配制pH=0.64三氯乙酸缓冲溶液。需加入多少摩尔强酸或强碱?
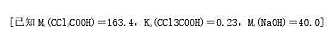
用NaAc?3H2O晶体,2.0mol/LNaOH来配制PH为5.0的HAc-NaAc缓冲溶液1升,其正确的配制是()。
A.将49克NaAc?3H2O放入少量水中溶解,再加入50ml2.0mol/LHAc溶液,用水稀释1升
B.将98克NaAc?3H2O放入少量水中溶解,再加入50ml2.0mol/LHAc溶液,用水稀释1升
C.将25克NaAc?3H2O放入少量水中溶解,再加入100ml2.0mol/LHAc溶液,用水稀释1升
D.将49克NaAc?3H2O放入少量水中溶解,再加入100ml2.0mol/LHAc溶液,用水稀释1升
若配制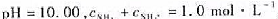 的NH4-NH4Cl缓冲溶液1.0L,问需要15mol·L-1氨水多少毫升?需要NH4Cl多少克?
的NH4-NH4Cl缓冲溶液1.0L,问需要15mol·L-1氨水多少毫升?需要NH4Cl多少克?
A.H3PO4⎯H2PO42-
B.H2PO4-⎯HPO42-
C.HPO42-⎯PO43-
D.H3PO4⎯PO43-