 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
298K下,对于反应:N2(g)+3H2(g)⇌2NH3(g),△rHmӨ=-92.2kJ•mol-1若升高温度,则:△rHmӨ和△rSmӨ()。(增大、减小或基本不变)
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298K下,对于反应:N2(g)+3H2(g)⇌2NH3(g…”相关的问题
更多“298K下,对于反应:N2(g)+3H2(g)⇌2NH3(g…”相关的问题
A.34.04kPa
B.43.54kPa
C.56.66kPa
D.156.0kPa
工业生产SO2Cl2(1)有以下两种方法:
SO2(g)+C(g)=SO2Cl2(1)①
SO2(g)+2HCl(g)=SO2Cl2(1)+H2O(1)②
(1)请根据热力学数据计算说明,欲得到更大的转化率,应采用什么路线更好?
(2)对于②反应,增大体系温度,对反应有什么影响?
(3)求反应①在298K时的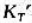
已知下列两个反应:
(1)2H2(g)+O2(g)=2H2O(1);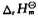 (298K)=-571.70kJ·mol-1
(298K)=-571.70kJ·mol-1
(2)2H2(g)+O2(g)=2H2O(g);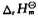 (298K)=-483.65kJ· mol-1
(298K)=-483.65kJ· mol-1
求298K时水的标准摩尔汽化热。
A.0.693倍
B.137倍
C.8.5倍
D.2倍
可逆反应 达到化学平衡时:
达到化学平衡时:
(1)升高温度,反应标准平衡常数(),其原因是();
(2)在温度不变的条件下压缩气体的体积而增大压力时,I(g)的解离度().其原因是();
(3)恒容条件下充入N2,I2(g)的解离度(),其原因是()。
(4)恒压条件下充入N2,I2(g)的解离度(),其原因是()。