 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
下列叙述中,哪一种情况适于沉淀BaSO4()?
A.在较浓的溶液中进行沉淀;
B.在热溶液中及电解质存在的条件下沉淀;
C.进行陈化;
D.趁热过滤、洗涤、不必陈化。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.在较浓的溶液中进行沉淀;
B.在热溶液中及电解质存在的条件下沉淀;
C.进行陈化;
D.趁热过滤、洗涤、不必陈化。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列叙述中,哪一种情况适于沉淀BaSO4()?”相关的问题
更多“下列叙述中,哪一种情况适于沉淀BaSO4()?”相关的问题
mol·L-1EDTA.试计算SO42-的质量分数.
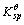 =1.1×10-10。
=1.1×10-10。
SCN)2和MgSO4溶液混合,观察到不同的实验现象, 试解释产生这些不同的实验现象的原因。

A.形成晶形物质的过程称为“结晶”
B.得到无定形物质的过程称为“沉淀”
C.从溶液中形成新相的角度来看,结晶和沉淀本质上是不一致的
D.从溶液中形成新相的角度来看,结晶和沉淀在本质上是一致的
A.蚯蚓的体壁有发达的肌肉,靠肌肉就能在土壤中运动
B.鸟的前肢变成翼,长骨中空,这些特点都与飞行相适应
C.鱼通过尾部和躯干部的摆动以及鳍的协调作用游泳
D.蝗虫有三对足、两对翅,善于跳跃、适于飞行
把CaCl2与Na2HPO4溶液混合时,可得磷酸八钙CasH2(PO4)6●5H2O晶体沉淀,把所得沉淀长时间加热可以水解生成羟基磷灰石结晶Cas(PO4)3(OH)。写出水解的反应方程式并讨论下列问题。
1.下列两种方法中,哪一种得到的羟基磷灰石多?为什么?
①1mol/dm3 CaCl2 50cm3 和1mol/dm3 Na2HPO4 30cm3 混合后,将所得
CagH2(PO4)6. 5H2O滤出。再将它放在80cm3水中于80°C加热5小时。
②lmol/dm3 CaCl2 50cm3和1mol/dm3 Na2HPO4 30cm3混合后,直接在80°C加热5小时。
2.在实验中,按①法制得的产物含Ca与含P摩尔比为1.5。计算CagH2(PO4)6中有多少摩尔百分比已转化为Cas(PO4)3(OH)?