 更多“分别计算下列反应的平衡常数,并讨论其方向.”相关的问题
更多“分别计算下列反应的平衡常数,并讨论其方向.”相关的问题
已知ϕθ(Cu2+/Cu+)=0.153V,ϕθ(I2/I-)=0.536V.
(1)计算ϕθ(Cu2+/CuI)的值.
(2)计算当c(Cu2+)=0.50mol·L-1,c(I-)=0.10mol·L-1时,反应2Cu2++4I-=2Cul+I2的标准平衡常数Kθ.
(3)判断在条件(2)下该反应的自发进行方向.[已知Kspθ(CuI)=1.27X10-12]
1073K时,在密闭容器中进行如下可逆反应:

反应的标准平衡常数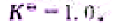
(1)如果反应开始时CO和H2O的分压都是100kPa,计算CO的平衡转化率;
(2)如果反应开始时CO的分压为100kPa,H2O的分压为500kPa,计算CO的平衡转化率。
用CaO(s)吸收高炉废气中的SO3气体,其反应方程式为
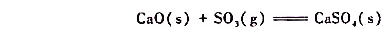
根据下列热力学数据计算该反应373K时的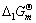 ,以说明反应进行的可能性;并计算反应逆转的温度,进一步说明应用此反应防止S03污染环境的合理性。
,以说明反应进行的可能性;并计算反应逆转的温度,进一步说明应用此反应防止S03污染环境的合理性。

可逆反应 达到化学平衡时:
达到化学平衡时:
(1)升高温度,反应标准平衡常数(),其原因是();
(2)在温度不变的条件下压缩气体的体积而增大压力时,I(g)的解离度().其原因是();
(3)恒容条件下充入N2,I2(g)的解离度(),其原因是()。
(4)恒压条件下充入N2,I2(g)的解离度(),其原因是()。
如图所示,无摩擦、无质量、无体积的活塞1,2,3将反应器隔成甲、乙、丙3部分,分别进行反应
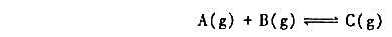
起始时物质的量已标在图中。某温度和100kPa下实现平衡时,各部分的体积分别为V甲,V乙,V丙。
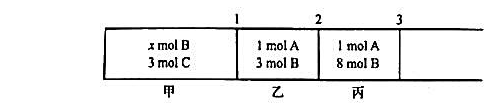
(1)这时若去掉活塞1,不会引起其他活塞移动,求算x值;
(2)去掉活塞2后再次达到平衡时,活塞3向哪个方向发生了移动?试通
过计算加以解释,可以假定反应的Kθ等于1。
A.增加SO2的浓度,正反应速率先增大,后保持不变
B.增加SO2的浓度,正反应速率逐渐增大
C.增加SO2的浓度,平衡常数增大
D.增加SO2的浓度,平衡常数不变
已知反应CO2(g)+H2(g)=CO(g)+H2O(g)在973K时的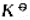 =0.618.若系统中各组分气体分压为p(CO2)=p(H2)=127kPa,p(CO)=p(H2O)=76kPa,计算此时
=0.618.若系统中各组分气体分压为p(CO2)=p(H2)=127kPa,p(CO)=p(H2O)=76kPa,计算此时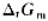 (973K)时值并判断反应进行的方向。
(973K)时值并判断反应进行的方向。
A.电对Fe3+/Fe2+做正极
B.反应Fe+2Fe3+=3Fe2+的平衡常数大约为8×1040
C.电池组成式为(-)Fe|Fe2+(c1)||Fe2+(c2),Fe3+(c3)|Pt()
D.电池的标准电动势为0.331V


 如果结果不匹配,请
如果结果不匹配,请 

















