 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对5%的食盐溶液含义的解释错误的是()
A.将5 g食盐溶于95 g水中所得溶液
B.100 g食盐溶液中含有5 g食盐
C.100 g水中溶解了5 g食盐
D.该溶液中溶质与溶液的质量比为1∶20
 答案
答案
C、100 g水中溶解了5 g食盐
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.将5 g食盐溶于95 g水中所得溶液
B.100 g食盐溶液中含有5 g食盐
C.100 g水中溶解了5 g食盐
D.该溶液中溶质与溶液的质量比为1∶20
 答案
答案
C、100 g水中溶解了5 g食盐
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对5%的食盐溶液含义的解释错误的是()”相关的问题
更多“对5%的食盐溶液含义的解释错误的是()”相关的问题
A.100g水中溶解了10g食盐
B.100g食盐溶液中溶解有10g食盐
C.将10g食盐溶解于90g水中所得的溶液
D.将食盐与水按1:9的质量配比的溶液
A.若有100g的食盐溶液,则含有10g氯化钠
B.将10g食盐溶解在90g水中所得溶液
C.100g水中溶解了10g氯化钠
D.将氯化钠与水按1 :9的质量配成的溶液
A.100克水溶解了10克食盐
B.100克食盐溶液中溶解了10克食盐
C.将10克食盐全部溶解于90克水中所得到的溶液
D.将食盐与水按1:9的质量比配制成的溶液
A.100克水中溶解了10克食盐
B.100克食盐溶液中溶解了10克食盐
C.将10克食盐溶解于90克水中所得的溶液
D.食盐、食盐溶液1:10质量比的溶液
A.5 g水受热变成5g水蒸气
B.5 g食盐溶解在95g水中,成为100 g食盐溶液
C.100 mL水加入100mL酒精,体积小于200 mL
D.木炭燃烧后质量减小
A.100g水溶解36g食盐恰好能配成饱和溶液
B.20℃时,100g食盐饱和溶液里含有36g食盐
C.20℃时,把136g食盐饱和溶液蒸干,可得到36g食盐
D.饱和食盐水溶液中溶质、溶剂、溶液的质量比为36:100:136
A.氧气和液氧都有氧化性 同种分子,其化学性质相同
B.食盐放到水里会逐渐消失 分子在不断运动
C.溶液间的反应比固体间的反应快 参加反应的粒子在溶液中接触机会比在固体中多
D.高架的电线夏天比冬天长 受热时原子之间的间隔增大
A.配制5%食盐溶液时,将称量的食盐放入烧杯中加计量的水搅拌溶解
B.铜结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅
C.测定未知NaOH溶液浓度时,酸式滴定管需用标准酸液润洗2—3次
D.配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释
A.属于混合物的是①②⑤⑦⑨⑩⑪⑫⑬
B.属于化合物的是③④⑥⑧⑭⑮
C.属于酸的是⑨⑮
D.属于盐的是⑧⑭
A.对刑法的解释结论并非都具有效力
B.任何刑法都有解释的必要
C.刑法解释可以超出刑法用语可能具有的含义
D.刑法解释是指对刑法规定的真实含义的说明
海洋中蕴含丰富的资源,下图涉及多个以海水为原料的生产流程。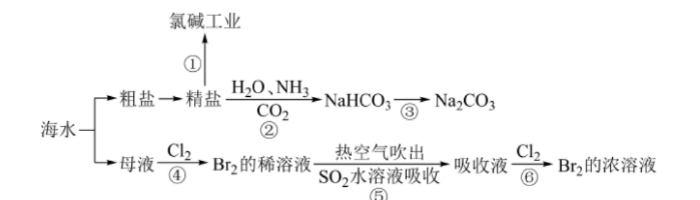 完成下列填空:
完成下列填空:
(1) 步骤①中电解饱和食盐水的化学方程式是()。
(2)工业上用Cl2与KOH(热溶液)制备KClO3,,Cl2+KOH=KCl+KClO3+H2O。配平上述反应方程式,并标出电子转移方向和数目()。
(3)关于卤素的下列说法错误的是()。
A、单质的熔点:Cl2>Br2>I2
B、元素的非金属性:Cl>Br>I
C、单质的氧化性:I2>Br2>Cl2
D、从海洋中获得Cl2,Br2的过程均涉及氧化还原反应
(4)对图中所示生产过程的说法正确的是()。
A、溶解度:NaHCO3>Na2CO3
B、第④⑤⑥步骤中,溴元素均被还原
C、第⑤⑥步骤的目的是进行溴的富集,提高Br2的浓度
D、联碱法与氨碱法相比,NaCl利用率较高,且能耗低
(5)步骤②是在饱和食盐水中先通入NH3再通入CO2,原因是()。
(6)某同学将CO2通入NaOH溶液中,当溶液呈中性时,溶液中浓度最大的微粒是()。
A、c(Na+)B、c(CO32-)C、c(HCO3-)D、c(H+)