 更多“调和颜色时需要加水稀释,减少原来的浓度以便上色。”相关的问题
更多“调和颜色时需要加水稀释,减少原来的浓度以便上色。”相关的问题
第1题
室温下,对于0.1mol/L的氨水,下列判断正确的是()
A.用相同浓度的硝酸与氨水反应时,硝酸体积小于氨水时,溶液可能呈中性
B.温度不变,加水稀释后溶液中c(NH4+)·c(OH-)不变
C.加水稀释后,溶液中导电粒子的数目减少
D.其溶液的pH=13
第3题
准确量取30.00ml弱酸,加水稀释至100ml。以为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被
准确量取30.00ml弱酸,加水稀释至100ml。以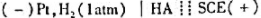 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。
第5题
准确量取30.00 mL弱酸HA,加水稀释至100.00 mL,在电池:(—)SHE|HA || SCE(+)中,以0.100 0 mol·L-1NaOH标准溶
准确量取30.00 mL弱酸HA,加水稀释至100.00 mL,在电池:(—)SHE|HA || SCE()中,以0.100 0 mol·L-1NaOH标准溶液滴定之。25℃时,当弱酸HA被中和一半时,电池电动势为0.524 V,化学计量点时,电池电动势为0.749 V。求:(1)弱酸HA的电离常数Kα值。(2)原弱酸HA溶液的浓度?(已知饱和甘汞电极的电极电位为0.244 V)
第8题
配制氢氧化钠标准溶液,要求()。
A.临用新配,用新沸放冷的水溶解
B.先配成饱和溶液,静置数日后,取上清液适量,有新沸放冷的稀释至所需浓度
C.为消除氢氧化钠中可能含有的少量Na2CO3,配制时需加少量HCI
D.标准液配制后应过滤
E.氢氧化钠加水溶解后需加热煮沸1h,以除去Na2CO3
第10题
二硫化碳(S2)的最小着火能量仅为0.0019mJ,因此虽然二硫化碳的密度大(比水重),但仍极危险。一般加水使(),以减少危险性。
A.遇水混合
B.液面上有水层封闭
C.液面上无水层封闭
D.形成稀释状态


 如果结果不匹配,请
如果结果不匹配,请 
















